Figyelmeztetés: ez a cikk, akárcsak előzménycikkei, olyan embereknek íródott, akiket laikusként érdekel a valóság és a világ szépsége, azaz a természettudományok, és szeretnének megérteni és átlátni dolgokat, érdeklődéssel fordulnak a világ, jelen esetben a farmakológia és a biokémia felé. Ökölbe szorult talpú, félanalfabéta, összeesküvés-elmélet hívő laposföldesek, akik sem arányokat, sem ok-okozati összefüggéseket nem képesek felfogni, és valójában se elolvasni, se megérteni nem akarják, mert kényelmesen elvannak konteóikkal, ne idegesítsék magukat vele feleslegesen.
Mint a cikksorozat legelején utaltam rá, a hagyományos gyógyszeripari vállalkozások mellett a molekuláris biológiai, biotechnológiai kutatások előrehaladásában a hidegháború éveiben nagyon komoly szerepe volt a két tömb biológiaifegyver-fejlesztéseinek, amelyek nemcsak irányokat jelöltek ki, hanem megoldási, fejlesztési lehetőségeket is feltártak, részben mellékhatásként, hiszen a mellékhatás az minden gyógyszerészeti és biokémiai kutatás fő hatása.
Közhely, hogy nemcsak a vegyiparban, hanem a gép-, energetikai-, híradástechnikai-, elektronikai iparban is az 1950 és 1990 közötti szédületes fejlesztést a katonai kutatások polgári területre történő „lecsorgása” indukálta, és a nyugat gyakorlatilag azzal verte meg a roggyant béketábort, hogy utóbbi, lévén nem volt piacgazdasága, ezeket a fejlesztéseket polgári oldalon nem alkalmazta. Ennek eredményét fogalmazta meg úgy a korabeli szovjet pénzügyminiszter nem sok szem közt, hogy olyan csórók vagyunk, hogy a cipőnk mellett járunk.
Kivéve a gyógyszeripart, ezért volt a magyar, az NDK és a szovjet gyógyszeripar nagyon is pariban a nyugattal. (És ezért csaptak rá 1990 után a tőkeerős nyugati vállalatok a magyar gyógyszercégekre is, mint gyöngytyúk a takonyra.)
Mikor az 1970-es évekre sikerült felderíteni az mRNS-ek funkcióját és többé-kevésbé – ekkor inkább még csak kevésbé – a működését, azonnal felmerült az ötlet, hogy ezeket a hírvivő molekulákat igénybe lehetne venni arra a célra, hogy az emberi szervezet bizonyos defektusait pótolják. Hogy ezekből oltóanyagot lehetne készíteni, ekkoriban még nem igazán merült fel, sokkal inkább az örökletes betegségek, enzimopátiák potenciális gyógyszereit látták bennük a kor kutatói. Rengeteg olyan betegség van, amelyet örökletes génhiba olyan módon okoz, hogy a szervezet biokémiai folyamatainak egy enzime hiányzik, és ekkor egy egész anabolikus vagy metabolikus ciklus értelmét veszti, nem működik, ahogy egy autót is meg lehet állítani egy üzemanyag-szivattyú kinyírásával, egy hűtővízcső átvágásával vagy az olajteknő kibökésével (kivéve a Trabantot…). Ilyen esetben az eljárás meglehetősen egyszerű, elviekben: nincs más dolog, mint az adott fehérjét termelni képes, de nem termelő, mert defektes génű sejtekbe bejuttatni a kérdéses fehérje genetikai kódját és rávenni, hogy mégis termelje. AZ első ilyen irányú kutatás 1977-ben a fenilketonuria, aki pedig ezt a csúnya női névnek tűnő szót nem tudja kimondani, annak PKU kiküszöbölésére irányult, természetesen az Egybesült Államokban. Mondjuk, ez felettébb egyszerűen hangzik (egy szívátültetés se bonyolult: ki kell venni a rossz szívet, és berakni a jót…), de számos gyakorlati buktatója van.
A fenilketonuria lényeg, durván egyszerűsítve, hogy az egyik aminosav, nem meglepő módon fenilalanin lebontása hibát szenved, mert az aminosav dezaminálása ugyan megtörténik (az ezt végző enzim jó), de a képződő ketont továbboxidáló enzim már nincs, ezért a szervezetben ez az anyag felhalmozódik, amit a delikvens kipisál (ezért „uria”, azaz vizelés). A dolog kicsit ördögi. Mert a fenilketonok bántalmazzák az idegszövetet, így szellemi visszamaradottságot, debilitást okoznak. Amennyiben a fenilalanint elhagyják az étkezésből, és a beteg nem tudja mérgezni magát...ez működik, de az egyrészt nem olcsó, másrészt nem gusztusos, mert valódi étel helyett csak mindenféle szintetikus löttyöt ehet, harmadrészt, mivel fenilalaninra pedig a testfelépítéshez szükség van, akkor a beteg girhes, belszervi problémás, stb. lesz, köpedelem fizikummal. Szóval, sehogy se jó. PKU-s gyerek van elég, a szellemi visszamaradottság kb. 1%-áért fele ez a betegség. (A hibás gént minden 50. ember hordozza, de recesszíven öröklődik.) Ezért adtak volna kísérleti gyerkőcöknek először mRNS-t, hogy ilyen módon az enzimet „leszintetizálják”. A dolog azonban már a kezdetek kezdetén felsült.
Mikor a kísérleti állatoknak intravénásan beadták az első, egyébként természetes úton nyert, mRNS-adagokat, ezek az állatkák rövid úton felfordultak. Miért történt ez? Ekkoriban még senki sem tudta, hogy a nukleinsavak ugyanúgy antigének, mint a testidegen fehérjék, azaz az immunrendszer felismeri őket, immunreakciót váltanak ki, a makrofágok illetve a dendritikus sejtek nekikesnek, mint tót az anyjának, és ennek következményei: gyulladás, láz, izomgyengeség, súlyos elesettség, majd súlyos esetben sokk, ami vérnyomáseséssel, a perifériás erek görcsével, végül pedig szívmegállással jár együtt. Ehhez nem szükséges mRNS-t befecskendezni. Ha valaki tudni akarja, miképpen megy, milyen érzés, milyen tünetekkel jár (erről is szó volt a cikksorozat korábbi részében) elegendő egy átlagembernek intravénásan beadni 5-10 ml nyers tehéntejet, garantáltan attól is felfordul – hiszen az is gyakorlatilag egy tömény testidegenfehérje-szuszpenzió - ez különösen januárban ajánlott, mert akkor legalább némi haszna is lesz a dolognak, hiszen a beálló 42-43 fokos lázával egy ideig még fűti a helyiséget, ahol megtér az Atyához. Érdekes, hogy ez nem egy elterjedt öngyilkossági módszer, pedig biztosan nem kevésbé fájdalmas, mint kénsavat inni. A „tiszta” nagy dózisú mRNS befecskendezés legalább akkora sikersztori, mint az afganisztáni háború, mert azon kívül, hogy a mellékhatás (az elpatkolás) megfelelő dózis esetén az immunreakció miatt minden esetben bekövetkezik, (100%) de a kívánt hatást meg az mRNS 0%-os biztonsággal érte el, mert először is, nem jut át a sejthártyán, azaz a keringésbe vitt mRNS-t a sejtek nem veszik fel, és a fel nem vett RNS-t a keringésben az ribonukleázok gyorsan felszabdalják (ha elég sok van beadva, akkor nem tudják olyan sebességgel, hogy hatás ne legyen veszedelmes), másrészt, ha pedig bejutott is volna, akkor se hatott volna, mert az mRNS finomszerkezetének ismeretének hiányában az első szintetikus mRNS-eket a szervezet testi sejtjei „nem tudják olvasni”, kb. annyit tudnak vele kezdeni, mint Kolompár Gazsi a Révai lexikonnal, szó szerint, azaz vagy eltüzeli (energetikailag hasznosítja) vagy kidobja. Ahhoz ugyanis, hogy az mRNS-en rögzített genetikai információt a sejt fehérjegyártói, a riboszómák alkalmazzák, leolvassák, egy megfelelő bázissorrend és megfelelő térszerkezet kell, amit akkoriban még senki se tudott. Ezért rövid időre az mRNS a fiókba került. Vakcinaként pedig mindenki az 1980-as évek elején először legyártott módosított vektorvírusokat kezdte el fejleszteni, amelyekről már e cikksorozatban is szó volt.
Nagyjából 1990 körül (dióhéjban ennyit „az mRNS vakcina annyira új, hogy csak na, ezért biztosan nem jó, mert még senki se vizsgálta alaposan” érveléséről) került ismét napirendre – ekkor már lényegesen magasabb genetikai és molekuláris biológiai tudás mellett – hogy létre kellene hozni mRNS hatású biotechnológiai készítményeket, és ezekkel legyártatni a szervezetben ezt-azt. Ez egyrészt megint a fegyverfejlesztők ötletelése volt – ha az az „ez-az” speciel valami rettenetes toxin, pl. botulotoxin, akkor igen csekélyke adag mRNS-el lehet extrém, az ismert mérgeknél nagyjából három-négy nagyságrenddel kisebb halálos adagú mérgeket létrehozni. Maga a szám valóban látványos: ha egy embernek beadnánk hatékony formában azt az mRNS-t, amely botulotoxint szintetizál, akkor ennek oly csekély lenne a halálos adagja, hogy nagyjából 4 gramm ki lehetne irtani a teljes emberiséget. Botulotoxinból ehhez megközelítőleg nyolc kiló kellene. (Összehasonlítás képpen: a Szovjet hadseregnek, orosz „biztos, ami biztos” alapon volt belőle vagy egy tonna…) A biológiai(vegyi) fegyver-fejlesztés ezen a téren azonban nem igazán volt sikeres, mert harctéren nem igazán működik egy olyan eszköz, amit mélyfagyasztva kell tárolni, és ami kb. attól hatását veszti, ha csúnyán ránéznek, és se orálisan, se bőrre jutva nem hat, be kő« szúrni. Így megint maradt az üzletileg kevéssé kifizetődő (de azért látjuk, hogy működik…) békevegyipari felhasználás, például lehet belőle vakcinát csinálni. Gyorsabban, rugalmasabban, körülményes biotechnológiai gyártás nélkül, teljesen szintetikusan, és ami a legfontosabb, ha van bevált gyártási technika, OLCSÓBBAN, mint a hagyományos-, vagy vektorvírusos oltások, és roppant célravezetően. Ez mindenki fantáziáját elkezdte izgatni a kutatók között, és miután elmagyarázták az igazgatóknak, hogy ez mennyi zsetont jelent, onnantól az övékét is. (Közbevetés: aki reggeltől estig gyalázza a gyógyszergyártókat azért, mert azok, úgymond, profitéhesek, biztosan úgy gondolja, hogy autót, kólát, vekkert, hajgumit vagy zsömlét a piaci szereplők merő emberbaráti szívjóságból, és nem profitért állítanak elő. És mindenkit megnyugtatok, hogy a vegyiparon belül a hagyományos kémiai gyógyszergyártás profitrátája nem kiemelkedő, a legmagasabb profit tisztítószerekkel és kozmetikumokkal, parfümökkel érhető el. Ja, meg narkóval.) A képlet egyszerű, elmondva különösen, megvalósítva már annyira nem: rakjunk össze egy működőképes mRNS-t, amely alkalmas arra, hogy az emberi sejtekben fehérje termelését indukálja.
Azt, hogy mi az mRNS, már tisztáztuk a cikksorozat III-IV-V. részeiben. Mivel azonban tíz emberből tizenkettő lusta visszalapozni, ezért röviden (röviden!) átvesszük még egyszer.
Az m, azaz messanger RNS-ek a sejtmagban (vagy a mitokondriumokban, vagy egyes elvetemült csúszómászóknál speciális esetekben csak úgy, ez utóbbi az un. génamplifikáció, de ez már tényleg komoly „patkolt biztosíték” a Teremtőtől, de ezek mellékszálak) képződik az átíró (transzkriptáz) enzim munkája során a DNS-ről. Hogy éppen melyik és mennyi szakasz hányszor íródjon át a DNS-ről mRNS-re, azt speciális szabályzófehérjék, megkapóan trükkös mechanizmusok útján szabályozzák, ezért az mRNS olvasásának már nincs szabályzója, egyszerűen arányosan annyi mRNS képződik, amennyi a sejt, illetve a szervezet (mert mondjuk az a sejt hormont, mediátort, drogot vagy egyéb nyalánkságot termel közhasználatú célokra) szükséglete, mármint, ha jól megy minden, azaz az mRNS mennyisége az, amely a fehérjeszintézist szabályozza. A sejtmagosok mRNS-ei mindig egyetlen egy fehérje tervrajzát, genetikai kódját tartalmazzák bázistriplettek formájában, és ez megfelel a DNS bázissorrendjének, amiről írták (az un. templátról), azzal a különbséggel, hogy timin helyett uracilok sorakoznak. Míg a riboszómák (az a a fehérjéket a sejtben előállító, két alegységből álló szép nagy, nagyjából makkra emlékeztető alakú összetett fehérjék) RNS-ei, a sejtmagok s-RNS-ei és az aminosavakat a riboszómához cipelő és beépítő t (transzfer) RNS-ek gyakran tartalmaznak úgynevezett ritka bázisokat, amelyek eltérnek a DNS-ben használt négy kódbázistól, addig az mRNS-ek nem. AZ mRNS-ek egy rövid, jellegzetes, 8-12 bázisból álló szignálszakasz után szép hosszan tartalmazzák a letöltendő fehérje kódját (baktériumok esetén előfordul, hogy költségtakarékossági okokból, bár ott nem Varga Miska a szakminiszter, több kisebb fehérjét egy mRNS-re írnak), majd a végén található egy átlag 30-60 bázisos végzóna, ami már nem kódol, majd egy un. palidrom szekvencia, (palidromoknak nevezzük azokat a szövegeket, kódsorrendeket, melyek mindkét oldalról olvasva ugyanazt jelentik, pl. az a szöveg, hogy „móni fara finom”) ami ezért összekapcsolódik egy rövid szakaszon önmagával, kettős láncot alkotva. Ennek az a szerepe, mint mikor a varrónő elvarrja az anyag végét, hogy ne feseljen fel, és úgy is néz ki. Ha ez a tűzött vég nincs meg, akkor a riboszóma nem olvassa az mRNS-t, mert erről az oldalról fűzi be, és ha ezt nem találja, visszadobja, mint az ótépé a hiteligényt. Ez nagyon fontos. Ez azt a célt szolgálja, hogyha az mRNS molekula megsérülne, szétszakadna, vagy két mRNS összetapadna, akkor a riboszómák ne kezdjenek el hülyeségeket gyártani, mint mikor egy vak talál egy reszelőt, és megtapogatja, és azt mondja, hát, ez biztos hottentottául van, nem értem. Tehát, egyrészt az mRNS-roncsokról nincs fehérjeátírás, másrészt pedig a palidrom nélküli mRNS-ről, tehát az első, még a nyolcvanas évek elején szült szintetikus mRNS-ek se működtek, a riboszóma nem ribiszóma, ilyen olcsón nem teszi szét magát. (De mint említettem, ez a korábbi cikkekben részletesebben olvasható.)
Mint mondottam, mRNS-ből kevés kell, annyira kevés, hogy a riboszómák rendszeresen osztoznak rajtuk, mint Marci kakason a tyúkok („a mi Marcink, drágám”) míg Vuk haza nem szállította, azaz az mRNS olyan hosszú, mint a sün pélója, és egy időben, egymás után több riboszóma is ráfűződik, és gyárt róla, azaz ahogy nekem brit oktatóm mondta Leedsben, úgy néz ki, mint a sebességmérő csomós kötél, amire a fehér brit gyerekek bólogattak, mint tengerészeti kultúra, a többi sügér kelet-európaiaknak meg idegesítően nagyokos és tudálékos nyuszinak kellett elmagyarázni, hogy mire is gondol az a jóember. (Aki nem tudná, a tengerészeti gyakorlatban a régi szép, multigender előtti időkben a hajók sebességét úgy mérték, hogy egy olyan kötelet dobtak a vízbe, amelyre csimbókokat kötöttek, a végén egy fa úszóval, és mérték, hogy meghatározott idő – fél perc - alatt hány csomó megy le a kötélen a vízbe, 1 kn/h megfelel egy tengeri mérföld/órának. Ebből okos ember már kiszámolhatja, hogy a csimbókok távolsága a kötélen kb. tizenöt méter negyven centi, (1/120 tmf)). Magyarán szólva, igazság szerint többnyire marha kevés mRNS elegendő. Valamelyik ráérő Watson-tanítvány annak idején kiszámolta, hogy egy átlagos E. coli sejtben mégis miből hány molekula van, és arra jutott, hogy mRNS-ből egy időben nagyjából nyolcezer. Már hogy nem fajtánként: összesen. Ehhez képest tessék összeadni, hogy egy Pfizer-oltással megközelítőleg-nagyságrendileg-kábé 1011 db mRNS-t tolnak be. Na jó, azért az emberi sejtek nemcsak nagyobbak, némileg bonyolultabbak is, mint egy hóhérkötél.
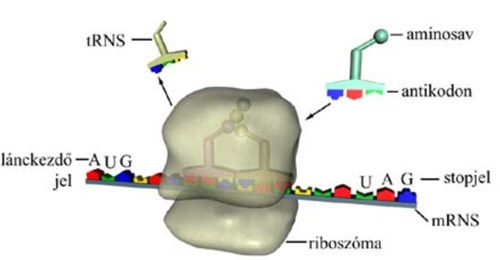
Egyszerűsített ábra arról, miképpen történik egy riboszómában a fehérjeszintézis. Forrás: tudasbazis.sulinet.hu
Mint a fentiekből kiderül, a lerongyolódott, elszakadt mRNS-ek nem működnek többé. Ez azért fontos – ennek a szennyvízből való covid-RNS-kimutatásban is szerepe van, mint a vonatkozó részben kifejtettem, ennek több köze van a vajákossághoz, mint a valós analitikához – mert az RNS-ek olyan csuda találmányok, hogy kb. száz bázissorrend nagyságú darabokban érzik jól magukat. Más szavakkal, ha rövidebb RNS-eket öntenek össze egy pohár lóhugyba, azok viszonylag rövid időn belül összetapadnak, ha hosszabbakat, azok meg elbomlanak. Ennek térszerkezetei okai vannak, mondja erre a biokémikus professzor, ami azt jelenti, hogy a lóf.sz se tudja, hogy ez miért következik be. A ritka bázisok azért vannak a többi RNS-ben, hogy merevítsék és stabilizálják őket (és természetesen azért, hogy speciális térszerkezetet biztosítsanak neki, amelyek a működésüket biztosítják) ezek hosszú élettartalmúak, míg az mRNS leginkább olyan, mint a százforintos boltban vett kínai termék, amely valójában nem PRC-ben, hanem Alsógagy településen készült, Encstől nem messze (igazi gagyi gyártmány). A legtöbb mRNS hatástartalma pár óra nagyságrendű, nagyon ritka, hogy napokig, pláne hetekig egzisztáljon egy sejtben. Muszáj is, hogy így legyen, mert mint említettem, az mRNS-ről a riboszómákban a fehérjegyártás már nem szabályzott, maga az mRNS képződése volt szabályzott, azaz ezeknek eliminálódniuk kell.
Mi mindent tud legyártani egy riboszóma? Kb. mint egy szovjet babakocsigyár, amely, ha megkapja a megfelelő alkatrészeket (ami mondjuk a szovjet érában nem egyszerű), tanktól sorozatvetőn át vadászgépig bármit. Más szavakkal, kis túlzással, de bármely sejtmagos élőlény bármely sejtjének bármely riboszómájának beadunk egy rendes, olvasható mRNS-t, az azt le fogja húzni, azaz emberi nyiroksejtekkel is lehet gyártatni kígyómérget, és nyúlseggsejttel lehet rókaszőr-kreatint, csak annyi kell, hogy a sejt működjön, és legyen elég energiája és aminosava. Persze, az se hátrány, ha az adott fehérjetermék nem mérgező a sejtre. Például, ha kiírom nekik CD-re, illetve bocsánat, mRNS-re a gyilkos galóca mérgét, az amatoxin-a-t, ami annyira nem vészes, mert nyolc aminosav, azaz 24 bázis az egész, és beadom egy májsejtnek, hogy ezt gyártsa le, hamar úgy jár, mint mikor a South Parkban Kenny ismerkedik a láncfűrésszel. Mindez azonban rövid ideig fog tartani, pontosan addig, míg az adott mRNS működik a sejtben.
Az mRNS sejtműködésben való felhasználásában 2004-ben történt áttörés, mikor amerikai kutatók, sok más intézet besegítésével – de egyébként szegediek is dolgoztak rajta, igen - megoldották azt, hogy az mRNS-t ne ismerje fel az immunrendszer antigénként, de a sejtben működjön. Egészen addig jól működött in vitro (a vitrinben, az üvegen, azaz a lombikban) az idegen mRNS, míg mikrotűvel beszúrták a sejtbe, (vagy később már elektroforézissel bekergették a szövettenyészetbe) és betolták, mint említett, in vivo (élőben) nem igazán, mert akinek immunrendszere van, azoknál nem, mert felfordultak. Az első kísérletekben immunrendszer-fosztott egereken vizsgálták: nem működött. Megint nem.
Ki kellett deríteni (kilencvenes évek második felében vagyunk) hogy a sejtek felületén un. mintázatfelismerő receptorok (TLR) vannak, amelyek dolga az, hogy észrevegye, hogy begarázdálkodott egy idegen RNS és hamis igét akar hinteni. Ezek reagálnak idegen DNS-re is, de a TLR 7 és TLR 8 feladata a sejtben lévő, vélhetőleg vírus eredetű idegen RNS felismerése és a vészcsengő megnyomása. Ekkor a sejt a már az előző részekben meghatározott módon részben riasztó citokineket küld ki a szervezetbe, részben védekezni kezd, ha pedig ez se sikerül, jön az apoptózis, mint mikor a matróz két százas szöget kér a kannibálfaluban, és megakadályozza, hogy a bőréből tamtamdob legyen. A sejt inkább elöli magát.
Hogy lehet ezt megcsinálni, hogy mégis működjön? Olyan módon, hogy az RNS láncán egyes bázisokat speciális, a természetben nem előforduló bázisokra cserélünk ki, hasonlóan ahhoz, ahogy ritka bázisokkal operálnak a t –, és r-RNS-ek. Olyan bázis kell, amelyet valamely természetes bázis helyett a riboszómában dolgozó enzim felismer, de az immunglobulinok meg nem tapadnak rá, és a sejten belüli TLR-ek sem veszik le róla, hogy ez egy RNS. Nem kellett sokat kipróbálni, csak vagy háromszázat, míg megtalálták a megfelelő bázist. Ez a mesterséges bázis az pszeudouridin és még jobb az 1-metil-pszeudouridin, amely szerkezetében igen hasonló a természetesekhez. Egyébként számos rákgyógyszert készítettek már olyan mesterséges nukleinsav-bázisokkal, melyek beépülnek a nukleinsavba, de a nukleinsav nem kettőzhető vagy nem lehet róla mRNS-t írni, így a sejtosztódás megáll, ezzel a daganat nem terjed. Ez az egyszerűbb, mert hogy NE működjön, az nyilván nem bonyolult (de kemoterápiás célokra csak korlátozottan, kombinált terápiákban hatékony), ennél kicsit nagyobb feladat, hogy de, működjön. Ez – mármint a metil-pszeudouridin -közvetlen szén-szén kötéssel rögzül az mRNS molekulára, nincs oxigénhíd, mint minden más aminosav minden más bázisánál, cukor-foszfor vázánál.
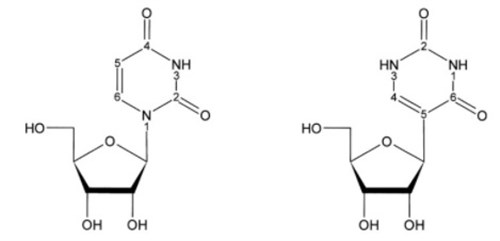
Míg az uridin (balra) nitrogén-szén, a pszeudouridin (jobbra) szén-szén kötéssel rögzül a nukleinsav láncán, így a nukleáz enzimek nem tudják lehasítani
Ennek a beillesztése után igen, működött, azaz a működésnek csakis annyi akadálya volt, hogy ne aktiválja az immunrendszert az RNS. Persze, ez szegény immunrendszer-fosztott egérkéket nem vigasztalta, hiszen az első kóbor baci elvitte őket kapálni. Arról nem olvastam, hogy hozzám hasonlóan perverz humorú biokémikus nem-e gyártatott mRNS segítségével széles spektrumú baktériumölő fehérjét, pl. lizozimot az immunfosztott egerekkel, hogy életben maradjanak (az első vírus-, vagy gombafertőzésig…).
(Ismét emlékeztetnék mindenkit arra, hogy ekkor, mire a pszeudouridinnel készített, a sejtműködésbe illeszthető mesterséges RNS elkészül, 2004-ben vagyunk, és már a következő évben oltottak klinikai vizsgálatként módosított mRNS-el állatokat, majd 2008-tól embereket, és eddig még senkit nem vitt el a rák, a polip meg a tintahal, és senkinek nem nőttek csápjai.)
Mivel minden élőlény minden DNS és RNS ligáza/polimeráza/hidroláza, transzkriptáza mind-mind hidroláz, azaz olyan enzim, amely az – O – kötést egy vízmolekula segítségével – OH HO- végekre, vagy a – N – kötést – NH2 HO- végekre (egy plusz hidrogént a gyűrűben lévő nitrogénatom az oxo-enol konfigzuráció megváltozásával „kölcsönöz” a gyűrűből) felbontja, ezért, az enzimek, ha meglátják a szén-szén kötéssel rögzített bázist, izzadnak, mint kurva a templomban, elfogy a tudomány, tehát az mRNS marad. Erről fehérjét lehet szintetizálni, de komplementert nem, mert az átíróenzimek nem működnek, azaz ilyen mRNS-ről a szervezetben másolat nem készülhet, semmiféle trükkel és húzással se.
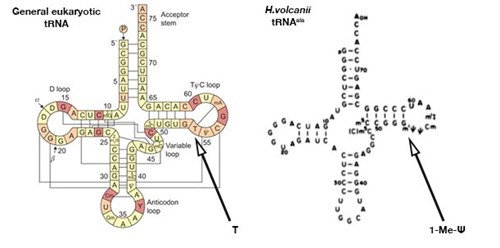
A t(transfer)RNS-ek speciális térszerkezetűek. Ezt úgy érik el, hogy ritka, a normál nukeinsavakban nem előforduló bázisokat tartalmaznak. Forrás: biology.stackexchange.com
Ebből egyenesen következik, hogy belőlük még annyi se kell, mint egy természetes mRNS-ből, mert igen hosszú ideig elműködgetnek egy sejtben. Egy idő után persze, egy másik bázisnál fel fognak szakadni, építőelemeik nagy része azonban más RNS szintézisére nem használódik fel, és a sejt vagy elbontja egy oxidázzal, de erre az emberi sejtek – a májsejtek kivételével – általában nem eléggé jól felszereltek, vagy egyszerűen kiengedi a keringésbe, ahonnét részben a májba kerülve elbomlik, részben kipisálódik. Nem képes semmiféle bajt csinálni. Legalábbis ilyen módon nem.
Tud-e az mRNS-ről genetikai információ átíródni az emberi DNS-re? Egyrészt a fenti okok miatt nem – nincs másolóenzim, ami meg tudná oldani, hogy a szén-szén kötéses bázisú mRNS-t szervezeten belül másolja – másrészt meg csak azért sem, mert ahhoz be kellene jutni a sejtmagba, ami nem olyan egyszerű. Jól néznénk ki, ha az élőlények nem védenék hatékonyan a genetikai információjukat, és a sejtmagba, fényképes belépőkártya nélkül, csak úgy, bárki, kedve szerint bedzsasztázhatna! Ez nem a magyar HM, ahol, mikor az embert leszerelik, a minisztériumi belépőt egyszerűen elfelejtik visszakérni. Ahhoz, hogy valaki bemenjen a sejtmagba, ugyanaz kell, mint mindenhova bemenéshez: vagy kulcs, vagy valami ágyúszerűség. Ágyúval be lehet menni, csak az is összetörik, ami mögötte van. A kulcs, ami engedi, hogy a sejtmag hártyáján ne az „access denied” felirat villogjon, kell a PIN kód, amit úgy hívnak, hogy nukleáris lokalizciós szignál (NLH), amely egy peptidvégecske, amellyel rendelkezik minden enzim és fehérje, akinek dolga van a sejtmagban. mRNS-t csak szállítófehérje visz ki a sejtmagból, és plusz nukleinsav-építőkövet is csak szállítófehérje visz be. Akinek nincs NLH-ja, mint a normál, mezei mRNS-nek, az a sejtmagba… nem… tud… (roncsolásmentesen)… bejutni. Egyébként pedig nem visznek magukkal nukleinsav-integráz enzimet se, amely kéne, hogy genetikai információt be tudjanak ollózni. Ez már négy.
Soha nem lesz képes beépülni. Oszt pont és jónapot.
Végezetül pedig, egyes nagyon speciális esetek és ritka kivételeket nem számítva RNS-ről az eukarióta sejtekben DNS-re ab ovo eleve nem íródhat át semmi, ehhez az így működő retrovírusok (lásd erről szóló cikket) speciális enzime, a reverz transzkriptáz szükséges, amely emberi sejtben nincs, nem termelődik.
Más szavakkal, három, egymástól teljesen független ok miatt nem történik, nem is történhet genetikai módosulás a sejtben. Ennek megértéséhez nem kell szakirányú egyetem, ez középiskolai biológiatudással is mindenki számára érthető kell(ene…), hogy legyen. Elég fájdalmas, ha nem az, de tudjuk, Magyarországon (is) a lakosság 80%-a nem tud megoldani egy másodfokú egyenletet. Ne kérdezzék, ezeknek hogy van érettségijük.
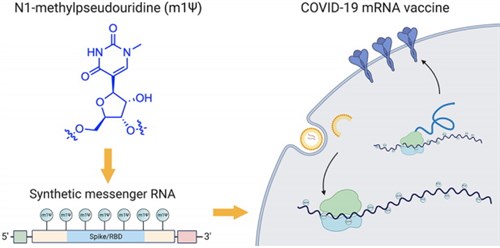
Az mRNS alapú vaksicinákat több cég, nem csak a gyógyszeriparban – akárcsak a többi covid-vakcina fejlesztő - BioNTech és Moderna fejlesztettek már állati vírusok ellen is, és a kétezres évek elejének SARS és MERS járványai (lásd az erről, a koronavírusokról szóló cikket) is dolgoztak ezen. Ezek a vakcinák konkrétan azért nem kerültek forgalomba, mert nevezett két koronavírus-járvány előbb megszűnt magától (pontosabban összefogott nemzetközi tevékenység hatására) minthogy használni kellett volna a védőoltást. Ez azért üzletileg nem volt éppen kellemes a fejlesztőknek, ezért most nem követik el ugyanezt a hibát. (Nagyjából ezt tapasztaljuk már 10 hónapja.) Konkrétan a SARS-Cov-2 nem sokban különbözik az említett előző kettőtől, csak járványosabb és kevésbé halálos, de a vírus felépítése és biokémiája lényegét tekintve kb. annyira különbözik tőlük, mint a kínai űrhajó a Szojúztól. Mikor 2020 januárjában megkezdték a covid-vakcinák fejlesztését, nem kellett a nulláról indulni, hanem kb. 80%-os készenlétről. Tisztázott volt a vírus szerkezete, hatásmódja, szaporodása, fertőzési mechanizmusa, célsejtjei, a tünetek nagyobb része, a toxikus hatások nagyobb része, az immunológia jelentős része. Ismert volt az mRNS vakcina készítés módja, ami kellett egyedül: a konkrét mRNS molekula megtervezése és létrehozása, és lipidhártyába illesztése. Ez nem véletlenül történt meg viszonylag nagyon gyorsan. Tulajdonképpen nem volt nehéz.
A metil-pszeudouridint tartalmazó mRNS lánc nagy stabilitású, a sejtbeli élettartama hosszú, és ezért róla átíródik a kérdéses S protein. Az mRNS módosítása elsősorban nem azt a célt szolgálja, hogy a sejten belüli élettartama hosszabb legyen, hanem azt, hogy a szervezet immunrendszere ne ismerje fel a molekulát antigénként, maga az mRNS ne váltson ki immunreakciót. Az immunreakciót majd az elkészült S protein, pontosabban S protein részlet váltja ki, mert a jelenleg forgalomban lévő mRNS oltások nem tartalmazzák a koronavírus teljes S proteinjének genetikai kódját, ahogy egyébként az adenovírus-vektorvakcinák sem, egyszerűen mert feleslegesen drága lenne. Forrás: ACS Central Science, Modifications in an Emergency: The Role of N1- Methylpseudouridine in COVID-19 Vaccines
A jelenleg ismert mRNS oltások nem tartalmazzák a teljes S protein genetikai kódját, éppen csak annyit, amennyi szükséges ahhoz, hogy az immunitás az S proteinnel szemben kialakuljon. Ugyanúgy, ahogy a vektorvakcinák (Astra-Zeneca, Szputnyik, Jansen) se. Az mRNS bemegy a sejtbe, az S proteinrészlet a sejtben több héten át termelődik (egyre csökkenő mennyiségben), majd, mivel a sejtnek nem kell, rájön, hogy tök feleslegesen gyártja, kidobálja: megjelenik a sejthártyán. Durván leegyszerűsítve itt találkoznak vele az immunsejtek, a helper T sejtek és a B sejtek, és „veszik le”, mint antigént (lád a vonatkozó részt a cikksorozatban), és alakul ki ellene a védettség. Az, hogy a termelt fehérje nem azonos a természetes Covid S proteinnel, nagyon fontos, mert maga az S protein önmagában nemcsak egy kötődésért felelős glikopeptid, hanem egyben toxikus is. A kialakuló tüdő-, szív-, emésztőszervi-, idegrendszeri károsodások jelentős részéért maga a toxinként viselkedő S protein a felelős. Ha az oltóanyag ezt tartalmazna, akkor az oltás ezeket a hatásokat hozná. Igaz, csak kismértékben, mert izomba adják, így csak izomsejtekbe és a legközelebbi nyirokcsomókba, ott a nyiroksejtekbe kerül be nagyobb mennyiségben, de erre nem lehet építeni, mert ha rosszul szúrják be, és emberi hiba bármikor lehetséges, akkor a vérkeringéssel már bárhová eljut. Éppen, mert maga az S protein egy toxin, a teljesvírusos oltások (Sinopharm) bejuttatható mennyisége korlátozott, még akkor is, ha a kérdéses protein bennük inaktivált. Ezért alacsonyabb az immunreakció szintje, és ezért, különösen idősebb, lanyhábban reagáló embereknél, korlátozottabb a védettség is. Az immunrendszer működése ugyanis – erről is szó volt az erről foglalkozó fejezetben (XV. rész) – nem egy kétállású kapcsoló, hogy igen/nem, és még csak az immunglobulinok vérszintje se jelent védettséget vagy nem védettséget (ajánlom figyelmébe ezt Toroczkai Lászlónak, ha az általa hivatkozott név nélküli szakértők ezt nem mondták el neki, de fogadom, hogy elmondták.) mert az immunitásnak a sejtes pillére legalább annyira fontos. Szóval: mRNS oltással olyan fokú immunreakció váltható ki, ami hagyományos oltással nem, ami védettségi szempontból jó, de mellékhatások tekintetében meg persze, rossz.
Ha valakit érdekel, hogy miképpen épül fel a Pfizer mRNS oltásának hatóanyaga (laposföldes: „nem tudjuk, mi van az oltásokban”), ez a molekula felépítése. Első szignál, a SARS-CoV-2 S proteinjének egy releváns részletének genetikai kódja, a hátsó szignál, a palidrom régió. Ennyi, le lehet másolni, aki akarja, az oltás azonban ezzel azonban nem kész, mert ezt be is kell csomagolni egy lipidhártyába, hogy hatékony legyen. Forrás: ACS Central Science, Modifications in an Emergency: The Role of N1- Methylpseudouridine in COVID-19 Vaccines
Miképpen jut be a sejtbe maga az adott mRNS molekula? Önmagában sehogy. Ahhoz, hogy ezt az ember megértse, ismerni kell az állati sejtek sejthártyájának a szerkezetét. (Itt szükséges zárójelben megjegyeznem, hogy linkeltek már be nekem olyan internetes anyagot, amelyet a nagyokos „szakértő” (laposföldes bugadoktor) arról beszél, miképpen halálos-rettenetes, ahogy az mRNS átmegy a „sejtfalon”. Nos, az állati sejteknek nincs sejtfala. Sejtfala csak a baktériumoknak, gombáknak, növényeknek van, glikoproteidből, cellulózból, hemicellulózból, kitinből, lipopoliszacharidból. Aki ennyivel nincs tisztában, az nem csodálható, hogy hülyeségeket beszél, és másokat hülyít.) Az állati sejtek sejthártyája is a Teremtő egyik jellegzetesen frappánsan ötletes munkája, amely alapszerkezete foszfolipidekből áll, azok kettős rétegéből. A foszfolipidek (pl. a lecitin) úgy néznek ki, hogy van egy hosszú szénhidrogén-láncuk, amely értelemszerűen zsírban oldódó (mert ők maguk a zsírok), apoláris, dielektromos állandójuk alacsony, és ehhez kapcsolódik egy poláris, ionizálódni tudó, vízben oldódó (hidrofil) fejrész, amely mondjuk zsírsavak esetén egy karboxilcsoport, lecitin esetén egy kolin-foszfát rész, stb. Ezért, ha ez olaj-víz határfelületen helyezkednek el ilyen molekulák, akkor hidrofil fejrészük a vízbe, lipofil farkuk az olajba megy, és kb. „összekötik” a két réteget. Így működik a szappan is, meg minden mosószer, és az élő szervezetek is tele vannak mosószerekkel, ilyen, így működő molekulákkal. Ha olajba juttatunk ilyen felületaktív anyagokat, összedugják buksi fejecskéjüket, és a lipoid farkukat kifelé fordítva képeznek cseppet, ha vízbe dobjuk őket, akkor pedig fordítva. Ezzel képesek zsírba vizet, illetve poláris anyagokat emulgeálni, vízbe pedig zsírokat, mert közöttük, mint sok bába között, elfér egy-két gyermek, azaz hasonló karakterű molekula. Egyébként ez a mosás, mint jelenség, a zsíros kosz vízzel lepucolásának lényege. A klasszikus szappan köztudomásúlag nem más, mint hosszú láncú monokarbonsavak nátrium-, kálium sói, és mint ilyen, az emberiség által előbb ismert, mint a dárda, a nyíl vagy a marihuána, mondhatjuk, ez volt az első vegyipari termék, mert összességében egy marék zsírt egy marék hamuval összefőzni nem nagy tudomány. Maga a „szappan” szó a kelta „sapo” ból ered, de semmi köze se Szapphohoz, se a leszboszikhoz, a leszboszi migránsokhoz is csak annyi, hogy 4000 éve a kelták is migráncsok voltak Európában, de ők már akkor is képesek voltak megmosdani.
A sejthártyák lényegében hasonló karakterű molekulákból felépülő kettős rétegek, amelyek kifelé-befelé hidrofil arcukat mutatják, befelé pedig lipidek, ezáltal a maguk vékonyságában is a sejt belső vízterét nagyon hatékonyan elzárják a külső víztértől, és ezen gyakorlatilag nem igazán tudnak más karakterű molekulák átjárni. A molekulák hidrofil fejei között nagyon erős másodlagos kötőerők vannak, amelyek nagy felületi feszültséget indukálnak, ezért kis mérettartományban egy ilyen csepp meglepően stabil, összefüggő, ugyanakkor teljesen „mintha folyadék” lenne (mert az is, végül is), ezért teljesen flexbilis. A szappan (pl. nátrium-sztearát vagy palmitát) keveset árt egy ilyen membránnak, mert a sejtmembrán belső felszíne negatívan töltött, így a sejtmembánba belekeveredő szappanmolekula, mivel azonos töltés, taszítja, kilökődik. Ellenben az úgynevezett kationos felületaktív anyagok, akik vízben oldódó „feje” pozitív töltést nyer, (benzalkónium, sterogenol, stb.) bele tudnak hatolni a membránba, és mivel idegenek a membrántól, szétszakítják. Ezért ezek a kationos mosószerek, un. invert szappanok erős fertőtlenítő hatással bírnak a mikróbákra, mert szétfolyik tőlük a sejt. Az elmúlt másfél évben lelkesen osztogatták őket koronavírus ellen kézfertőtlenítésre, felületfertőtlenítésre, „mert ezek igen jó fertőtlenítők”, azt elfeledve (vagy nem is tudva), hogy a vírusoknak, fájdalom, de nincs sejthártyájuk, merthogy nem sejtek, ezért ezek a szerek vírusokra kb. alig hatnak, de hát az emberiség X. alkalommal bebizonyította a „járványkezelés” során, hogy nemcsak hülye, hanem kincstári vigyorral csinálja ugyanazt, ami száz éve, a spanyolnátha-járvány idején se használt semmit se.
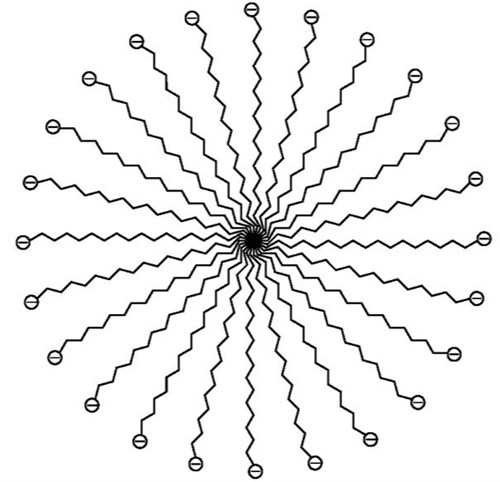
A szappan molekulái (pl. nátrium-palmitát vagy -oleát) vizes oldatban hidrofil „fejükkel” a vizes közeg felé fordulva, lipoid „farkukkal” egymáshoz simulva képeznek kolloid csomót, un. micellákat (ez is középiskolai kémiai anyag). Ez a lipoid csepp képes felvenni más zsíros anyagot is, ezen alapul a szappan tisztító, nedvesítő, diszpergáló, nedvesítő hatása. A sejthártyák ennek a micellának a kétrétegű, dupla óriásai. A felületaktív anyagokat az ércflotációtól kezdve a tűzoltó habokon át a vízbázisú kenésig a műszaki gyakorlatban kiterjedten alkalmazzák, de a legfontosabb „felhasználása” maga az élővilág. Csak ilyen módon biztosítható gazdaságosan vízoldható és zsíroldható struktúrák egymás mellé és egymásba építése. Forrás: sulinet tudásbázis.
Ameddig stabil ez a fajta membrán, az kb. 100 mikrométer nagyság, ami kb. be is határolja, hogy mekkora lehet max. egy állati sejt, egy-két trükktől eltekintve. Az ember legnagyobb sejtje a petesejt, kb. ekkora. Léteznek ennél nagyobb egysejtűek, de azoknak pl. kova-, vagy mészvázuk is van, mint pl. a páncélos ostorosoknak...mondjuk, ők nem igazán állatok, de ezt a mellékszálat végkép hanyagoljuk. A sejthártya úgy néz ki, hogy ez a membrán, amelybe különböző nagy fehérjék, ioncsatornák, un. G fehérjék, receptorfehérjék (mint pl. a kovid-gyűjtögető ACE-II) vannak beágyazva. Anyagforgalom alapvetően szabályozott módon ezen kapufehérjéken át történik. Mondjuk, van anyag, amely át tud menni a membránon... például az alkohol! És akkor a sejt végre jól érzi magát. De a membránon át többnyire fagocitózissal lép be valamiféle anyag.
A sejtek egy igen jelentős része képes arra – egy amőba vagy egy fagocita – hogy kvázi körülfollya és bekebelezze a nálánál kisebb sejtet, fehérjét, törmeléket, bármit. A fagociták pl. nemcsak baktériumokat, hanem tustintát is esznek, ezért halványul el lassan a tetoválás, ha olyan helyre kerül, ahol hozzáférnek. Kisebb mértékben azonban a legtöbb sejt tud bekebelezni dolgokat. Ezt használják ki a vírusok is, mikor „ráveszik” – megfelelő receptorhoz kapcsolódás és enzimaktiválás után – hogy az adott sejt bevegye őket magába.
Az mRNS oltások működőképességéhez elengedhetetlen, hogy maga az mRNS molekula beágyazásra kerüljön apró, néhány nm méretű lipoid mátrixba, mely lipidcseppek képesek „beleolvadni” magába a sejthártyába, ezzel az mRNS-t bevinni a sejtbe. Ha e nélkül, egyszerű fiz. só oldatban adnák be őket…mivel módosítottak, így immunreakciót nem váltanának ki….ott állnának tanácstalanul, mint Ádám anyák napján, és különösebb élettani hatás nélkül a májban szétszednék őket. Ezért kulcsfontosságú a nyert mRNS belekeverése a lipidmátrixba, és ezzel van kapcsolatban az, hogy az mRNS vakcinák eltarthatósága a hagyományos-, és vektorvakcinákéhoz képest rossz, ezért igénylik a stabil mélyhűtést, és azt, hogy 2-8 fokon adva mielőbb, leginkább 48 órán belül beadják őket. Ha a lipidmátrix stabilabb és emulgeálószereket is tartalmaz, mint a Moderna oltása, viszonylag jól eltarthatóak -20 C fokon is, ha egyszerű lipidemulzió, mint a Pfizeré, akkor mélyfagyasztást igényelnek, ahol kvázi már elhanyagolható a hőmozgás, ez pedig leginkább folyékony nitrogén, de mivel szállítani értelmesen és gazdaságosan csak szárazjégben lehet leghidegebben (és a repülőgépeken már az is bajos, míg az ADR/RID szerint a szárazjég nem veszélyes aru, addig a légiközlekedésben ICAO szerint annak minősül, hiszen a zárt légterű repülő egy kicsit más, mint egy nyitott kamion) , ezért megelégednek a „csak” -80 C fokos tárolásával és szállításával. Ez is bajos. Maga a Pfizer vakcina gyári kiszerelése is egy eléggé ukmunfuk, kifejezetten tömegoltásra kitalált valami. Nem arra találták ki, hogy egy háziorvos szép csendesen a rendelőjében oltogasson vele. A 0,7 ml-es egységampullát fiziológiás sóoldattal fel kell hígítani, elméletben hét, a gyakorlatban az üveg kialakítása miatt hat embert lehet egy ampullából oltani – ehhez oltópont kell, segédszemélyzet, egy asszisztens, aki hígít, kimér, előkészít, egy másik asszisztens, aki adminisztrál, meg egy harmadik ember, aki a hűtő meg a mélyfagyasztó között közlekedik. Tipikusan arra találták ki, hogy oltóállomásokan, tömegeket oltsanak be vele.
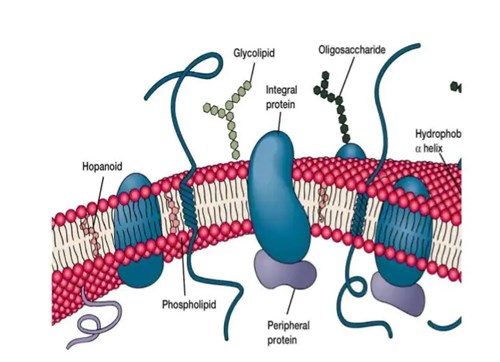
Sejthártya felépítése. A foszfolipidek alkotta kettős rétegben fehérjék vannak beágyazva, amelyek a sejt működését biztosítják, de maga a térelhatároló elem a kettős rétegű foszfolipid. Forrás: Ultraestructura bacteriana (slideshare.net)
Miből van ez a lipidcsepp? A sejtalkotó foszfolipidek, pl. a lecitin nem igazán jók erre a célra, egyszerű technikai okból: olyan nagy a fajsúlykülönbségük a vízhez képest, hogy a velük képzett partikulák nem adnak stabil emulziót. Ha valakit érdekel az, hogy milyen az, mikor apró zsírcseppek többé-kevésbé stabilan emulgeálva vannak vízben, az öntsön magának egy pohár tejet. A tejzsír a vízben ugyanígy oszlik el. Stabil? A teszkó gazdaságos, míg be nem rohad, biztos, de a tehénből kifejt aligha, ha valaki kiteszi egy köcsögben a kamrába, vagy belemászik a macska, vagy feljön a tetejére az ó, vajon miért így elnevezett tejföl, amely kb. a tej zsírtartalma. Ezért az mRNS vakcinák szabadalmának fontos része, e nélkül nem lehet – a legjobban kitalált RNS nélkül se – hatékony oltóanyagot készíteni, a lipidmátrix összetétele, és a két komponens egyesítésének technológiája, mert e nélkül a dolog nem működik.
Ha valaki vesz egy deci olajat, meg egy deci vizet, és összerázza, azt fogja tapasztalni, hogy az kb. másodpercek alatt elválik egymástól, azaz hiába keveri össze a leghatásosabban, pl. turmixgéppel, az emulzió akkor is viszonylag gyorsan szétválik, és ez a szétválás kifejezetten gyors, ha nagy a fajsúlykülönbség, azaz pl. majdnem hármas fajsúlyú tetrabróm-etánt akarunk vízzel összekeverni, nem pl. benzolt. Ha azonban un. emulzióstabilizátorokat (az élelmiszeriparban pl. glicerin-monozsírsav-észtereket) adnak a rendszerhez, meg lehet oldani, hogy az adott olaj/víz emulzió meglepően stabilis legyen. Például így gyártunk hidratáló kenőcsöket („keverj-kavarj, nem kell ész, legyél fiam, gyógyszerész”, ahogy a SOTE gyógyszerészkar természetesen nem hivatalos, de ott mindenki által ismert jelmondata tartja), de így készülnek olyan speciális, rémisztő képződmények, mint például a puding, a tejszínhab, a majonéz, vagy a fúrózagy, a borotvahab, nipaq ipari robbanóanyagok, valamint a fehér, keresztény, heteroszexuális férfi, mert kb. nyolcvan másodpercig tudnánk életben maradni emulzióstabilizátorok nélkül (ennyit bírna kenés nélkül a mellhártyánk légzés közben). Mivel a nukleinsavak erősen polárisak, vízben jól elvannak, így az mRNS lipidburokba csomagolásához olyan keverékanyag kell, ami több komponensű, és amely tartalmaz olyan lipoid farkciót, amely beleoldódik a sejthártyába, és olyan „fél-lipidet” amely összekapcsolja a lipoid frakcióval magát az mRNs-t, és emulzióstabilizátort, ami lehetővé teszi, hogy a nagyjából 0,1 mikrométernél is kisebb lipidgömböcskék legalább egy korlátozott ideig (2-8 fokon tartva két napig) ne tapadjanak össze, és váljanak el a vizes fázistól. A vizes fázist természetesne egy fiziológiáshoz közelítő sóoldat képviseli, mint hordozóközeg. A Pfizer oltásában ez kálium-kloridot, dikálium-hidrogén-foszfátot (pH szabályzásra) konyhasót, nátrium-dihidrogén-foszfátot (szintén pH szabályzásra) tartalmaz, és egy olyan rettenetes mérget, amely, biztosan állíthatom, a nyugati világban évente több millió embert öl meg. Az a neve, hogy cukor. A Moderna oltásában a vizes közeg egyszerű ecetsav-nátrium-acetát puffer, kevés sóval, szintén cukorral felengedve, azaz kb. megegyezik azzal, amiben a salátát szoktuk elkészíteni. Ez utóbbi jobb az emulzióstabilizálásra, de kevéssé szövetbarát, ezzel magyarázható, hogy a Moderna oltása hevesebb szöveti reakciót és az oltás helyén fájdalmasabb piros foltot hagy, pár órára, viszont az oltóanyag tárolhatósága meg sokkal jobb.
(Folytatása következik.)